Od 8. 12. 2020 poteka globalno množično cepljenje z različnimi cepivi proti virusu Sars-CoV-2. V Sloveniji se je cepljenje pričelo 27. 12. 2020.
Trenutno so pri nas v uporabi cepiva proizvajalcev Pfizer/BioNTech, AstraZenece in Moderne. Vsa tri cepiva so dobila pogojno dovoljenje za promet, ker uradno ni drugega zdravljenja. Za vsa tri cepiva potekajo številne študije, ki so v različnih fazah kliničnih raziskav. Študije še niso zaključene, zato še nobeno od teh cepiv nima uradne odobritve in licence.
V III. klinični fazi običajno sodeluje nekaj tisoč oseb, do 6. 4. 2021 pa je bilo na svetu porabljenih 693 milijonov odmerkov cepiv proti Sars-CoV-2, pomeni 9 odmerkov na 100 ljudi. Večina cepljenih (sodelujočih) tako ni bila vključena v dvojno slepe randomizirane študije, kar je pogoj za III. klinično fazo.
Razvoj cepiv je kompleksen in dolgotrajen proces, ki povprečno traja 10 do 15 let. Kljub uspešnemu sodelovanju številnih znanstvenikov, spoznavanju virusa ali njemu podobnih virusov, skrajševanju administrativnih postopkov in neomejenim finančnim sredstvom pa obdobja nekaj let, ki je potrebno za skrbno spremljanje in ugotavljanje (poznih) neželenih učinkov, ne moremo skrajšati na nekaj mesecev. Mnoge od študij bodo zaključene šele leta 2022 ali celo 2023.
1. Klinične študije in koronavirusna cepiva
1.1. Stopnje razvoja in testiranja, ki veljajo za cepiva
Začetek: raziskave v laboratoriju in na živalih
Raziskovalna faza: vključuje osnovne laboratorijske raziskave, traja 2-4 leta. Raziskovalci opredelijo naravno ali sintetično substanco, ki bi lahko preprečila ali zdravila bolezen.
Predklinična faza: običajno vključuje raziskovalce v privatni industriji, traja 1 do 2 leti. Raziskave potekajo na celičnih ali tkivnih kulturah in živalih. Preučujejo varnost in imunogenost potencialnega cepiva ali zmožnost, da bi povzročilo imunski odgovor. Teste opravljajo na laboratorijskih miškah ali opicah. Raziskovalci dobijo osnovne podatke o celičnih odgovorih, ki bi jih lahko pričakovali pri človeku. Za prihodnje faze lahko predlagajo potencialno varen odmerek cepiva in varen način vnosa. Razvoj mnogih potencialnih cepiv se ustavi v tej fazi, ker ne izzovejo željenega imunskega odgovora.
Vloga za raziskovanje novega zdravila: sponzor je običajno privatno podjetje, ki pošlje Vlogo za raziskovanje novega zdravila (Investigational New Drug Application) na agencijo za zdravila (v ZDA U.S. Food and Drug Administration-FDA, v Evropi European Medicines Agency-EMA). Navede postopek pridobitve in testiranja, povzame rezultate laboratorijskega dela in opiše predlagano raziskavo. Raziskovalna komisija ustanove, kjer bo potekala raziskava, mora odobriti klinični protokol raziskave. Agencija za zdravila mora odobriti Vlogo v 30. dneh.
Nadaljevanje: klinične raziskave na ljudeh
Faza I: prvi poskus ocene potencialnega cepiva pri ljudeh poteka na majhni skupini odraslih, 20-80 oseb. Če je cepivo namenjeno otrokom, ga najprej preizkusijo na odraslih, nato stopenjsko v nižjih starostnih skupinah. Prva faza je lahko ne-slepa (non-blinded ali open-labeled) in pomeni, da raziskovalci in morda udeleženci vedo, ali uporabljajo cepivo ali placebo. Udeležence strogo spremljajo. Namen te faze je ocena varnosti cepiva in določitev vrste in stopnje imunskega odziva.
Faza II: sodeluje nekaj 100 oseb. Nekateri lahko pripadajo skupini s tveganjem, da pridobijo bolezen. Razporeditev v skupino, ki dobi cepivo oziroma skupino, ki dobi placebo je naključna (randomizirana). Namen te faze je ocena varnosti in imunogenosti cepiva, predlagan odmerek in način cepljenja (aplikacije).
Faza III: sodeluje 1000 do nekaj 1000 oseb. Testi so randomizirani in dvojno-slepi (niti raziskovalci, niti udeleženci ne vedo, ali so prejeli cepivo ali placebo). Cepivo primerjajo s placebom, ki je lahko fiziološka raztopina, drugo cepivo ali druga substanca. Namen te faze je ocena varnosti (nekateri stranski učinki se v majhni skupini ne pokažejo) in učinkovitosti cepiva. Ali cepivo prepreči bolezen? Ali prepreči okužbo s patogenom? Ali povzroči tvorbo protiteles?
Odobritev in licenca: po uspešni fazi III razvijalec cepivo opremi z etiketo/oznako. Agencija pregleda tovarno, v kateri bo proizvedeno in potrdi oznako. Cepivo dobi licenco.
Zaključek: nadzorovanje cepiva po pridobitvi licence
Faza IV: so opcijske raziskave, ki jih opravi podjetje, ki izdeluje cepivo. Z njimi nadaljuje s spremljanjem varnosti in učinkovitosti cepiva.
VAERS: ameriški CDC in FDA sta leta 1990 ustanovila The Vaccine Adverse Event Reporting System, z namenom odkrivanja stranskih učinkov v morebitni povezavi s cepivom. Vsako leto je zabeleženo približno 30000 dogodkov, 10 do 15 % je resnih, ki zahtevajo hospitalizacijo, so življensko nevarni ali povzročijo smrt. Je sistem za prostovoljno poročanje.
Dogodek lahko prijavijo zdravstveni delavci, pacienti, njihovi starši ali prijatelji. CDC dogodek razišče in skuša ugotoviti, ali je bil naveden stranski učinek dejansko povezan s cepivom. CDC navaja, da obravnavajo podatke iz VAERS z namenom, da bi: odkrili nove, nenavadne ali redke stranske učinke cepiva; opazili porast že zananih stranskih učinkov; opredelili potencialne dejavnike pacienta za določen stranski učinek in ocenili varnost novo licenciranih cepiv. V študiji opravljenimi med leti 2006 in 2010, z namenom izboljšanja programa cepljenja, so ugotovili, da se prijavlja manj kot 1 % neželenih učinkov cepiva.
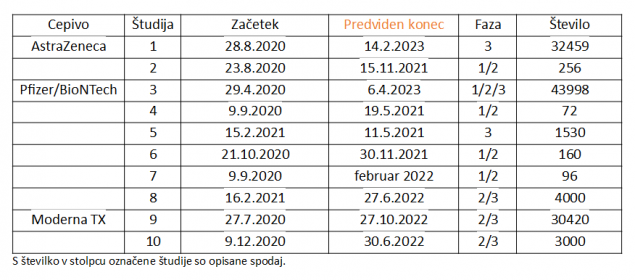
1.2. V svetu poteka veliko študij na področju koronavirusnih cepiv. Približno 60 jih je v fazi kliničnega testiranja, več kot 100 pa v predklinični fazi. Navajamo nekaj najbolj aktualnih in predviden termin njihovega zaključka.
A. AstraZeneca (Vaxzevria)
1. Phase III Double-blind, Placebo-controlled Study of AZD1222 for the Prevention of COVID-19 in Adults , klinična faza 3, ciljno število 32459 udeležencev, začetek 28. 8. 2020, predviden zaključek 14. 2. 2023
2. Study of AZD1222 for the Prevention of COVID-19 in Japan , klinična faza 1/2, ciljno število 256 udeležencev, začetek 23.8.2020, predviden zaključek 15.11.2021
Napovedana je raziskava, v katero bodo vključeni otroci; klinična faza 2, predvidena vključitev 300 otrok, starih od 6 do 17 let, iz VB. Približno 240 jih bo dobilo CoV-19 cepivo, preostali v kontrolni skupini meningokokno cepivo; ocena varnosti in imunogenosti
B. Pfizer/BioNTech (Comirnaty)
3. Study to to Describe the Safety, Tolerability, Immunogenicity, and Efficacy of RNA Vaccine Candidates Against COVID-19 in Healthy Individuals , faza 1/2/3, ciljno število 43998 udeležencev, začetek 29.4.2020, predviden zaključek 6. 4. 2023; ocena varnosti, tolerančnosti, imunogenosti in učinkovitosti pri zdravih posameznikih v starosti 12 do 85 let
4. First-In-Human Study To Evaluate Safety, Tolerability, And Pharmacokinetics Following Single Ascending And Multiple Ascending Doses of PF-07304814 In Hospitalized Participants With COVID-19, klinična faza 1/2, ciljno število 72 udeležencev, začetek 9. 9. 2020, predviden zaključek 19. 5. 2021; ocena varnosti, tolerančnosti in farmakokinetike doz udeleženih, hospitaliziranih s COVID-19
5. A Phase 3 Study to Evaluate the Safety, Tolerability, and Immunogenicity of Multiple Production Lots and Dose Levels of BNT162b2 Against COVID-19 in Healthy Participants , klinična faza 3, začetek 15.2.2021, ciljno število 1530 udeležencev, predviden zaključek 11.5.2021; ocena varnosti, tolerančnosti in imunogenosti pri zdravih osebah v starosti 12 do 50 let.
6. Study to Evaluate the Safety, Tolerability, and Immunogenicity of an RNA Vaccine Candidates Against COVID-19 in Healthy Japanese Adults, klinična faza 1/2, ciljno število 160 udeležencev, začetek 21.10. 2020, predviden zaključek 30.11.2021; ocena varnosti, tolerančnosti in imunogenosti pri zdravih odraslih Japoncih v starosti 20 do 85 let.
7. A Trial Investigating the Safety and Effects of One BNT162 Vaccine Against COVID-19 in Healthy Adults, klinična faza 1/2, ciljno število 96 udeležencev, začetek 9. 9. 2020, predviden zaključek februar 2022; ocena varnosti in imunogenosti pri zdravih osebah v starosti 18 do 55 let, opcijsko tudi 56 do 5 let.
8. Study to Evaluate the Safety, Tolerability, and Immunogenicity of SARS CoV-2 RNA Vaccine Candidate (BNT162b2) Against COVID-19 in Healthy Pregnant Women 18 Years of Age and Older , klinična faza 2/3, ciljno število 4000 nosečnic, začetek 16. 2. 2021, predviden zaključek 27. 6. 2022; ocena varnosti, tolerančnosti in imunogenosti pri zdravih nosečnicah od 18. leta dalje.
Napovedana je raziskava, v katero bodo vključeni otroci; klinična faza 1/2/3, predvidena vključitev 4644 otrok, starih od 6 mesecev do 11 let, iz ZDA in Evrope. Prvi rezultati predvideni v drugi polovici leta 2021; ocena varnosti in imunogenosti
C. Moderna TX
9. A Study to Evaluate Efficacy, Safety, and Immunogenicity of mRNA-1273 Vaccine in Adults Aged 18 Years and Older to Prevent COVID-19, klinična faza 2/3, ciljno število 30420 udeležencev, začetek 27.7.2020, predviden zaključek 27. 10. 2022; ocena učinkovitosti, varnosti in imunogenosti pri zdravih odraslih ali osebah s stabilno kronično boleznijo, starosti 18 in več let.
10. A Study to Evaluate the Safety, Reactogenicity, and Effectiveness of mRNA-1273 Vaccine in Adolescents 12 to <18 Years Old to Prevent COVID-19 (TeenCove), klinična faza 2/3, predvidena vključitev 3000 mladostnikov, starih od 12 do 18 let, začetek 9. 12. 2020, predviden zaključek 30. 6. 2022; ocena varnosti, reaktogenosti in učinkovitosti.
Pri otrocih je predvidena še ena raziskava; klinična faza 2/3, predvidena vključitev 6750 otrok, starih od 6 mesecev do 12 let, iz ZDA in Kanade. Imenovana KidCOVE.
D. Povezava z okvirnimi načrti za otroško populacijo
2. Povezave na strani beleženja stranskih učinkov eksperimentalnih COVID-19 cepiv
2.1. Nacionalni informacijski center National Vaccine Information Center (NVIC) zbira podatke v zgoraj omenjeni VAERS podatkovni bazi. Dostop do podatkov o stranskih učinkih po cepljenju s COVID-19 cepivi v ZDA do 26. marca 2021 je na tej povezavi.
2.2. Povezava na britanski MHRA (Medicines and Healthcare products Regulatory Agency); na koncu dokumenta (prosim poglejte pod Annex 1) so povezave do prijavljenih možnih stranskih učinkov v povezavi s cepljenjem glede posameznega proizvajalca cepiva. Sum na stranske učinke v povezavi s cepivom lahko prijavijo zdravstveni delavci in zainteresirana javnost preko sheme Coronavirus Yellow Card reporting site, ki je bila vzpostavljena maja 2020. Zadnje poročilo navaja prijave od 9.12.2020 do vključno 21. 3. 2021. Skupno je bilo podanih 40883 prijav za cepivo Pfizer/BioNTech (vključuje 116627 neželenih učinkov), 99817 prijav za cepivo AstraZeneca (vključuje 377487 neželenih učinkov) in 379 prijav, ko vrsta cepiva ni bila navedena. Vključene so prijave smrti v kratkem času po cepljenju; 283 primerov po cepivu Pfizer/BioNTech, 421 po cepivu AstraZeneca in 9, ko vrsta cepiva ni bila navedana. Kolikšen odstotek stranskih učinkov po cepljenju je dejansko poročan v sistem, kot tudi kolikšen delež prijavljenih stranskih učinkov je s cepljenjem povezan, nam ni znano.
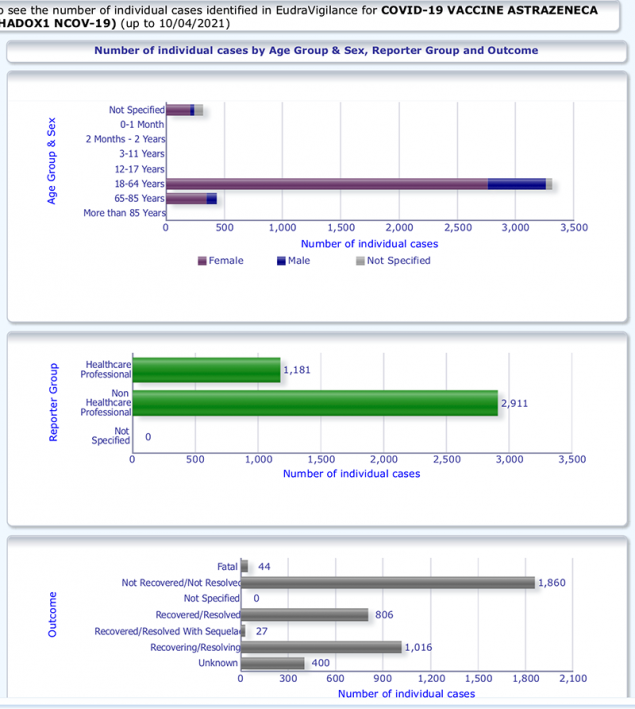
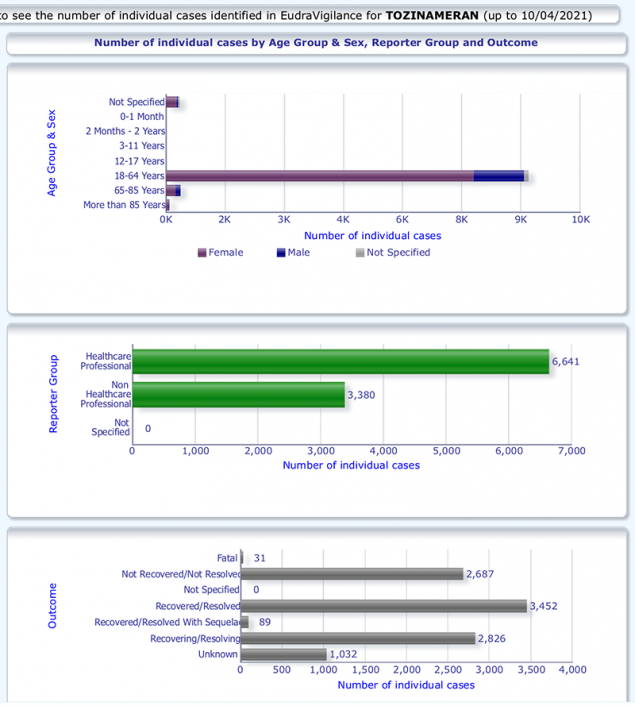
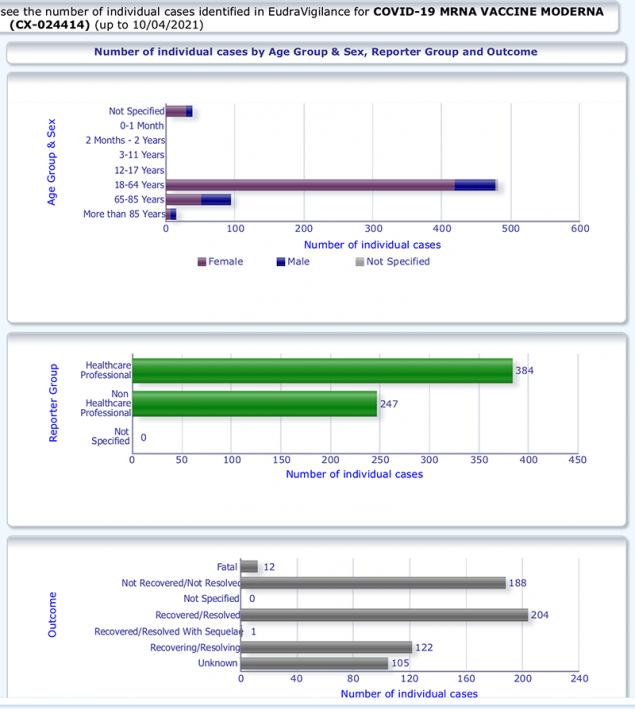
2.3. EudraVigilance je podatkovna baza, ki jo je pred leti vzpostavila EMA z namenom javnega dostopa do podatkov v poročilih o neželenih učinkih zdravil. Omogočeno je elektronsko poročanje s strani državnih regulatorjev za zdravila in s strani farmacevtskih podjetij. Tozinameran je Pfizerjevo koronavirusno cepivo.
2.4. V Sloveniji zdravniki poročajo o možnih neželenih učinkih cepljenja v eRCO (Elektronski register cepljenih oseb in neželenih učinkov po cepljenju). Prijava je možna v elektronski obliki, če je cepljeni že zaveden v sistemu. V kolikor cepljenje še ni zavedeno, se prijava posreduje na papirnatem obrazcu. Ni nam poznano, da bi o sumu na neželene stranske učinke v povezavi s cepljenjem lahko v sistem poročalo tudi drugo zdravstveno osebje ali javnost, kot je to možno v ZDA in VB.
Preberite še ostale objave o Covid-19:
- Norveški znanstvenik dokazal, da je bil koronavirus ustvarjen v laboratoriju Koliko smrti ‘zaradi’ koronavirusa je posledica uporabe respiratorjev?
- Koronavirus: Švedska bo naslednji mesec dosegla kolektivno imunost
- Koronavirus: prekomerna uporaba razkužil vodi v odpornost mikrobov
- Resnična zgodba: Osamljenost ubija bolj kot koronavirus
- Ali lahko sonce (UV žarki) uniči koronavirus?
- Zaradi korona ukrepov najbolj nastradali otroci s posebnimi potrebami in njihovi starši
- Cink vas ščiti pred korona virusom
- Koronavirus: kako okrepiti imunski sistem in se zaščititi
- Koronavirus: če ste se cepili za gripo, ste še posebej v nevarnosti
- Korona virus: če imate krvno skupino 0, ste najbolj odporni; če A, najbolj ogroženi
- Test za korona virus nezanesljiv: polovica je lažno pozitivnih (+ nekaj prikrivanih dejstev)
- OPOZORILO! Ibuprofen vam lahko zelo poslabša korona virus
- Na plan prihaja čedalje več dokazov, da so bile smrti ‘zaradi’ Covid-19 krepko napihnjene
- Nekaj dejstev, ki jih morate vedeti o različnih maskah in njihovem (ne)delovanju
- Študija: večina populacije ima naravno odpornost na COVID-19
- Oprostite, tukaj maske niso dovoljene!
- Posledica COVID-19 izolacij bodo tudi katastrofalni dolgoročni učinki na duševno zdravje mladih
- Uporaba razkužil vodi v kronično obstruktivno pljučno bolezen (KOPB)
- Oblasti priznavajo, da so desetine tisoče testov za koronavirus štele dvojno
- Pomanjkanje vitamina D ima ključno vlogo pri smrtnosti COVID-19
- Dr. Sebastijan Piberl: ‘‘Kot zdravnik ne morem mimo dejstva, da je to ignoranca medicinskega znanja“
- Dr. Gregor Knafelc: “Znanost ni nezmotljiva, sploh če je odvisna od politike in virov financiranja“
- Testiranje korone: pozitivni rezultati za papajo in koze
- Vrhunski švedski epidemiolog Johan Giesecke: “Izolacije in karantene so velika napaka!”
- Karantena in izolacija: tako brutalno so bile pretepene (in nekatere tudi umorjene)
- Italijanski imunolog: “Virus se bo ‘ugasnil’ sam, kmalu se bomo lahko vrnili v normalno življenje“
- Virolog osvešča: ni dokazov, da bi se virus prenašal po trgovinah, restavracijah ali frizerjih
- Vitamin C najboljše zdravilo za COVID-19; z njim zdravijo celo v newyorških bolnišnicah
- Koronavirus: strokovnjaki opozarjajo, da nošenje mask poveča nevarnost za infekcijo
- Koronavirus: v Veliki Britaniji prepovedali oglaševanje mask zaradi zavajanja
- Švedska: se je njihov pristop k ‘pandemiji’ izkazal za najboljšega?
- Korona: ko zaradi prehladnega virusa propadajo gospodarstva, družine in posamezniki
- Dr. Vladimir Pirnat: Karantenaa in drugi ukrepi slabijo imunski sistem oz. povečujejo umrljivost
- Dr. Vladimir Pirnat: diagnoza COVID na osnovi PCR testa je strokovna napaka
- Dr. Uroš Dobnikar: COVID 19: Javni poziv zdravnikom in Zdravniški zbornici Slovenije
- Vse, kar morate vedeti o PCR testih, s katerimi testirajo na koronavirus [VIDEO INTERVJU]
- Poročilo: Kar 90 % pozitivnih na covid-19 sploh ni kužnih
- Test za koronavirus predrl možgansko pregrado in puščati je začela cerebrospinalna tekočina
- Podporniki covid ukrepov uporabljajo psevdo psihologijo za šikaniranje “nevenikov”
- Belgijski zdravniki zahtevajo preiskavo lažne covid ‘pandemije’ in svetovne zdravstvene organizacije
- SCAMDEMIC 2020: Česa vam “lamestream” mediji in indoktrinirani strokovnjaki ne povedo?
- Umrl prostovoljec, ki se je javil za testiranje cepiva za COVID-19
- COVIDu-19 se lahko zahvalimo, da gripe in prehlada ni več
- Detektivska igra: Kdo v resnici ubija okužene s COVID-19?
- Slovenski zdravniki: Poziv k ustavitvi razgradnje sistema javnega zdravstva
- Dr. Sabina Senčar: Odprto pismo ministrici za izobraževanje, znanost in šport
- Dr. Vladimir Pirnat: Javno pismo Zdravniški zbornici Slovenije in replika na odgovor prof. dr. Ihana
- COVID-19 ukrepi: ko je ‘zdravilo’ bolj uničujoče kot sama bolezen
- Harvardski epidemiolog: Zapiranja držav so katastrofalen eksperiment
- Drugi val, ista strategija: Švedi vztrajajo pri ohranjanju človekovih pravic (in ponovno uspešno)
- Zdravniki svarijo: zaradi nošenja mask se lahko bojimo epidemije bakterijskih pljučnic
- Covid-19: politizacija, korupcija in zatiranje znanosti
- COVID pacient s sepso ‘čudežno’ okreval po prejetju megadoze vitamina C
- 10 kritičnih napak v znanstvenem članku, ki je podlaga za uporabo PCR testov
- Zdravilo za COVID-19 obstaja (in to celo več njih)
- Predavanje dr. Simone Gold: Resnica o cepivu za COVID-19
- Znanstveniki odkrili še eno zdravilo za COVID-19
- Študija: Vitamin D za zdravljenje koronavirusa zmanjša smrtnost za kar 60 odstotkov
- Mladoletni otroci preko skrbnikov vložili pobudo za ustavno presojo obveznega nošenja mask
- Stališče Iniciative slovenskih zdravnikov glede uporabe mask v obdobju ‘pandemije’ Covid-19
- Kirurg razbil mit: “Če maske ne delujejo, zakaj jih potem kirurgi nosijo?”
- Raziskava: COVID-19 cepiva na osnovi mRNA in tveganje za prionsko bolezen